В центре фармацевтической биотехнологии университета штата Иллинойс в Чикаго в первый раз создана синтетическая рибосома, трудящаяся в живой клетке. Продолжительное время такая процедура считалась находящейся за пределами отечественных технических возможностей и познаний. Сейчас она стала новой страницей в истории развития биотехнологий.
В середине девятнадцатого века бременский обозреватель Фридрих Энгельс обрисовал жизнь как метод существования протеиновых тел, неизменно обменивающихся с окружающей средой. Не обращая внимания на спорную формулировку, в этом определении отражены главные черты отечественных организмов и других живых существ: постоянная необходимость и белковая природа в материале для действенного синтеза протеинов.
Молекулярная и клеточная биология – относительно юные отрасли науки, но как раз с ними связаны прорывные разработки в области биотехнологии за последние годы. Проект “геном человека” помог выработать методики стремительного секвенирования и компьютерного анализа нуклеотидных последовательностей. Генетики определили язык ДНК, обучились просматривать а также корректировать замысел внутриклеточного синтеза белка, но работа с кодом – только начало.
Компьютерная модель рибосомы (изображение: rna.ucsc.edu).
Руководить самим синтезом протеинов возможно только в том случае, в то время, когда от понимания шаблонов по их выпуску мы перейдём к воссозданию всех стадий самого процесса производства. Исходя из этого детальное изучение механизмов трансляции создание и белка рибосом с нуля воображает на данный момент главный интерес.
Рибосомы – основная внутриклеточная фабрика белка. Структура этих органоидов в общем была известна в далеком прошлом, но не было человека, кто знал, как возможно заменить их молекулярной машиной. Создать специальную рибосому с нуля для производства экзотических полипептидов – и вовсе казалось задачей отдалённого будущего. Любая рибосома складывается из двух субъединиц, имеющих разную массу. Для синтеза белка обе субъединицы объединяются и скользят на протяжении матричной РНК, делая сборку полипептида по записанной на ней программе.
В ролике ниже мРНК представлена жёлтой нитью. Она выделяется через поры ядра в цитоплазму клетки. В том месте к ней сперва присоединяется малая субъединица рибосомы (голубой-), а после этого – громадная (фиолетовая). К появившемуся комплексу поступают молекулы аминоацил-тРНК (зелёные) поставляющие различные аминокислоты для синтеза белка. Скоро от рибосомы отделяется красная нить – синтезированный полипептид.
Неестественная рибосома, названную Ribo-T, устроена мало в противном случае. Если бы её сделали кроме этого складывающейся из двух частей, то синтетические субъединицы имели возможность перемещаться по матриксу эндотелия и вступать в конкурентные отношения с естественными, блокируя их. В итоге клетка бы, потеряв свойство синтезировать белки.
Исходя из этого авторы изучения решили заблаговременно объединить субъединицы неестественной рибосомы, покинув между ними пространство, достаточное для скольжения матричной РНК. Такая иммобилизованная структура демонстрирует менее впечатляющие результаты по скорости, но основное – она трудится в живой клетки E.coli. Бактерии выживают и продолжают синтезировать заданный белок кроме того по окончании замены всех исходных рибосом синтетическими.
«Скорость синтеза белка на Ribo-T получается приблизительно в два раза ниже, чем у естественных рибосом, но структура последних совершенствовалась в течении миллиардов лет эволюции, а отечественной разработке всего год», – комментирует соавтор изучения Александр Мэнкин (Alexander Mankin).
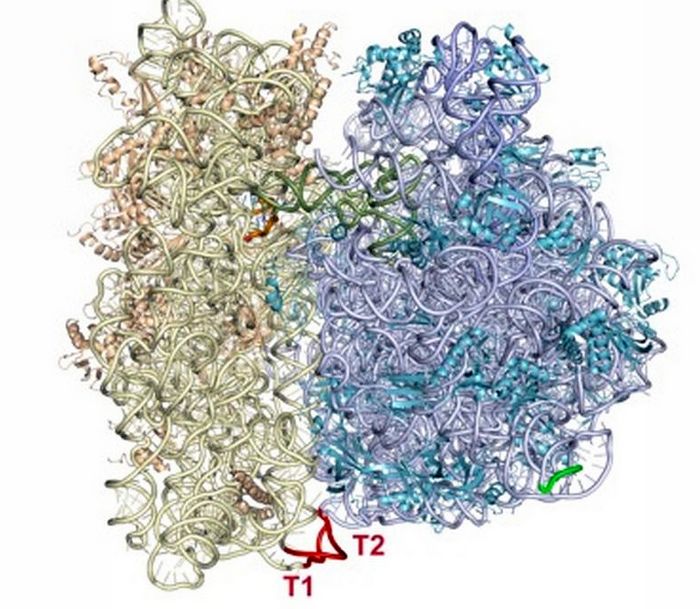
Структура неестественной рибосомы (изображение: Nature / Orelle, et al.).
В первую очередь восьмидесятых годов прошлого века для промышленного синтеза инсулина, соматотропина, интерферонов и других сложных белков употребляются бактерии (в основном E. Coli) с модифицированным геномом. При помощи неестественной рибосомы авторы рассчитывают изготавливать каждые белки ещё легче.
До тех пор пока любая Ribo-T способна синтезировать лишь протеины определённого класса, но для уровня доказательства концепции этого даже больше чем нужно. Следующим этапом развития биотехнологий будет создание универсальной синтетической рибосомы, талантливой делать сборку любых белков на заказ. Это смогут быть компоненты с любой биологической активностью – не которые содержат возбудителя надёжные вакцины, пептидные гормоны, компоненты селективных лекарств, новых косметических средств и пищевых продуктов.
“В собственной работе авторы преодолели главное препятствие для всецело синтетических рибосом с заданными особенностями, – отмечает научный сотрудник Лос-Аламосской национальной лаборатории Карисса Санбонмацу (Karissa Sanbonmatsu). – они заложили фундамент для драматических трансформаций”.
Схожую оценку даёт и биолог Йельского университета Фаррен Айзекс (Farren Isaacs): «Это изучение станет ключом для производства совсем новых классов экзотических протеинов», – говорит он в интервью изданию The Verge.
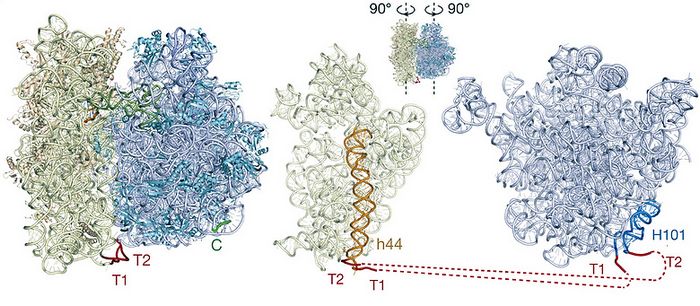
Образование связи между субъединицами в синтетической рибосоме (изображение: nature.com).
Годом ранее в НИИ Скриппса (TSRI) был создан новый генетический алфавит с парой дополнительных кодирующих молекул, не видящихся в природе. Сейчас его возможно опробовать на неестественной рибосоме.
Приобретаемые по сей день рекомбинантные белки были полностью аналогичны образующимся естественным путём. Они постоянно содержали остатки стандартного комплекта из двадцати либо менее L-альфа-аминокислот. Сочетая дополненный генетический код с возможностями неестественных рибосом, теоретически возможно запустить синтез 172 аминокислот и создавать в промышленных масштабах полностью другие белки.
Как и каждая научная разработка, неестественные рибосомы смогут стать разработкой двойного назначения. В случае если решить задачу их доставки в клетки живого организма, то
Ribo-T возможно будет применять для лечения отравлений рицином. Данный протеиновый яд не имеет своеобразных антидотов. Он разобщает субъединицы рибосом, блокируя синтез белка. Неестественная рибосома уже на данный момент устойчива к действию рицина, потому, что её субъединицы изначально связаны между собой.
Иначе, посредством Ribo-T смогут быть синтезированы новые токсины – полностью малоизвестные потенциальному сопернику и значительно более подходящие для диверсий, чем рицин и другие природные яды.