Учёные из НИИ Скриппса (TSRI) в Калифорнии модифицировали бактерию E. coli, введя в код её плазмидной ДНК два новых комплементарных соединения, не видящихся в природе. Так научная несколько взяла первый в мире полусинтетический живой организм и окончательно поменяла генетику. Одним из авторов работы указан отечественный соотечественник – научный сотрудник Денис Малышев. Он получал образование Столичном химическом лицее, по окончании чего окончил Российский химико-технологический университет им. Д. И. Менделеева и эмигрировал в Соединенных Штатах.
биохимиков и Современных биологов в полной мере можно считать программистами. Так как они освоили самый низкоуровневый язык, что лишь возможно представить, – генетический код. Прямое вмешательство в него похоже на реверс-инжиниринг. Оно произошло совсем сравнительно не так давно и совершило настоящий переворот в биотехнологиях.

Норман Борлоуг спас миллиард людей от голодной смерти посредством селекции (фото: guim.co.uk).
Приблизительно до восьмидесятых годов XX века селекционеры действовали вслепую, опираясь на закономерности и внешние признаки их наследования. Кроме того таким неоптимальным методом иногда совершались необычные по своим масштабам успехи. К примеру, лауреата Нобелевской премии Нормана Эрнеста Борлоуга именуют «отцом Зелёной и Белой революции» за то, что он смог вывести риса и сорта пшеницы с необыкновенной урожайностью. Согласно данным ООН, это уже спасло от голодной смерти около миллиарда человек и помогло сохранить само существование Мексики, Пакистана и Индии.
Время от времени способ ошибок и проб приводил к досадным просчётам. К примеру, не считая томатов урожайности новых и повышения картофеля сортов, в них увеличивался уровень содержания токсинов, обычных для всего семейства паслёновых. Такие сорта забраковывались, но никто не имел возможности вернуть годы израсходованного времени. Неприятность сдерживания генетики состоит как раз в страхе перед сложными разработками, а не в опасности самой поменянной ДНК. Так как любой организм (не считая собственного собственного) есть для нас генетически чужеродным.
Новые биотехнологические способы разрешают избежать аналогичных неточностей, сходу внося в генотип контролируемые трансформации. Кроме растений, данный способ активно используется у бактерий, потому, что, не считая собственной ДНК, они содержат ещё и удобную для работы плазмидную. Модифицированные штаммы преобразовываются в завод по производству сложных белков, самый востребованных в медицине. Среди них имеется инсулин, эритропоэтин, интерферон и другие. Согласно данным ВОЗ, один лишь генно-инженерный инсулин выручает от смерти сотни и тяжёлых осложнений миллионов человек во всём мире.
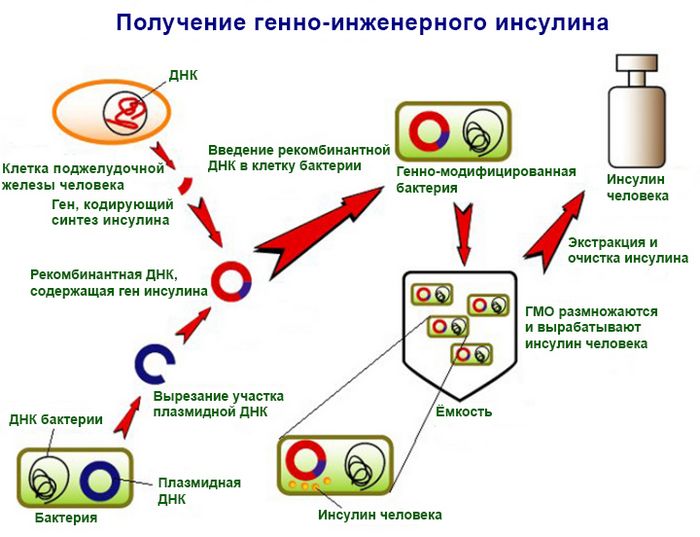
Схема получения инсулина способами генной инженерии (по данным: discoveryandinnovation.com).
Сейчас уровень качества нашей жизни зависит от того, как скоро мы сможем разобраться в подробностях синтеза белка и обучиться руководить этим процессом. Несложных способов трансформации генома уже не хватает: требуется расширять сам язык генетического программирования, вводя в него новые операторы. Именно это и произвели в университете Скриппса, объединив результаты научных работ по данной теме за более чем двадцатилетний период.
В природе нуклеиновые кислоты всех живых существ содержат лишь четыре азотистых основания: гуанин (G), аденин (А), тимин (Т) и цитозин (С) в ДНК, плюс неметилированную форму тимина (урацил – U) в РНК. Любой участок из трёх последовательно расположенных оснований формирует кодон, в котором и зашифрована команда на синтез определённой аминокислоты, или сигналы “старт/стоп”.
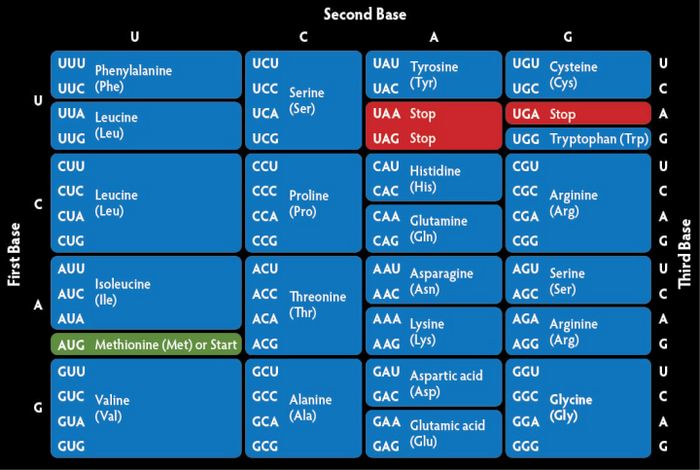
Схема кодирования аминокислот в ДНК (изображение: mpnforum.com).
При громадном химическом разнообразии аминокислот как группы веществ, белки любого живого организма состоят всего из двадцати L-альфа-аминокислот. Их положение определяет структуру протеинов и их биологические особенности.
Этот код характеризуется избыточностью: кое-какие аминокислоты смогут кодироваться различными методами. К примеру, к синтезу аргинина в клетки приведёт запись CG*, где * – любое третье основание. Исходя из этого, не обращая внимания на трёхбуквенную совокупность, в ходе синтеза белка образуются не 64=43, а всего двадцать различных вариантов аминокислот. Редко видящиеся селеноцистеин, пирролизин и другие «нестандартные» альфа-аминокислоты не нарушают этого правила. Они выпадают из неспециализированного перечня, поскольку образуются в противном случае – путём модификации одной из главных аминокислот уже по окончании её синтеза.
В лабораторных условиях, кроме AT(U)GC, возможно применять и другие кодирующие молекулы – такие как d5SICS и dNaM. Добавление всего пары синтетических соединений к стандартному комплекту азотистых оснований практически создаёт новый генетический алфавит. С его помощью возможно закодировать синтез уже не двадцати, а ста семидесяти двух аминокислот. Число новых вариантов белка, что возможно синтезировать из них, делается легко астрономическим.
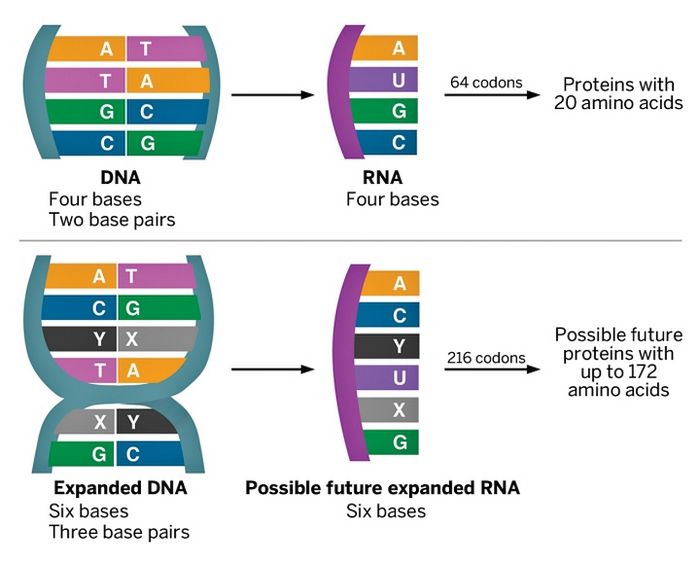
Всего два новых соединения расширяют диапазон синтеза вероятных аминокислот с 20 до 172 (изображение: cen.acs.org).
“В принципе, мы имели возможность бы кодировать совсем новые белки, сделанные из не видящихся в природе аминокислот, – поясняет начальник группы Флойд Ромсберг (Floyd E. Romesberg). – Это дало бы нам бо?льшую власть, чем когда-либо. Мы имели возможность бы приспособить разработку для протеиновых терапевтических и диагностических средств, лабораторных реагентов и многого другого. Такие нюансы применения, как наноматериалы, также вероятны”.
Соединения d5SICS и dNaM связываются между собой через гидрофобные сотрудничества, тогда как природные образуют водородные связи. Это не мешает применять их для расширения генетического алфавита, но создаёт последовательность преодолимых трудностей.
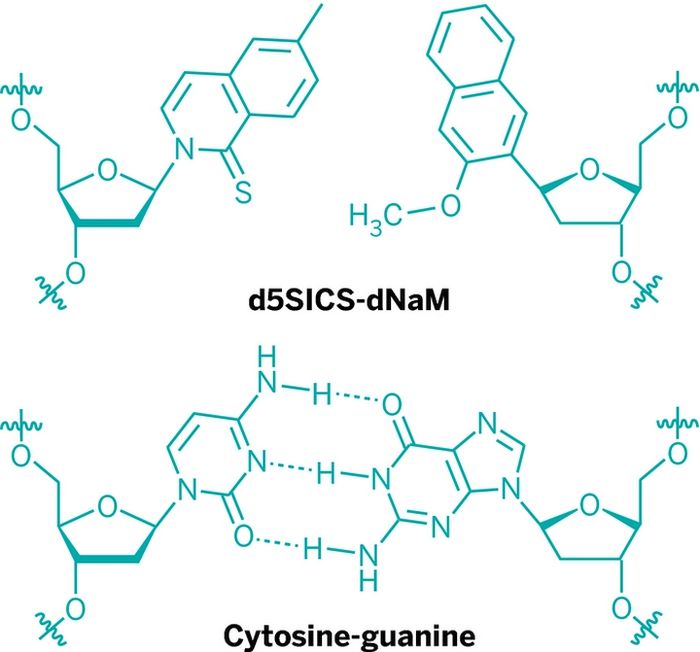
Сравнение связей синтетических (d5SICS-dNaM) и природных (C-G) оснований (изображение: nature.com).
Экспериментальный штамм бактерий с поменянным генотипом содержит эти два новых основания и сохраняет жизнеспособность, но пока не даёт потомства самостоятельно. Для размножения модифицированных бактерий требуется последовательность ручных манипуляций с раствором – таких как добавление фосфатных соединений, приобретаемых из водорослей.
«Принципиально важно подчернуть, что это кроме этого снабжает контроль над совокупностью, – говорит Денис Малышев. – Отечественные новые соединения смогут поступать в клетку лишь при помощи белков-переносчиков. Без них клетка возвратится к стандартному комплекту ATGC, а молекулы d5SICS и dNaM провалятся сквозь землю из её генома».
Авторы изучения рассчитывают, что в будущем найдётся метод создать всецело синтетический и способный к размножению штамм бактерий. Для этого требуется подобным методом увеличить «алфавит» РНК и, быть может, поменять сами рибосомы.